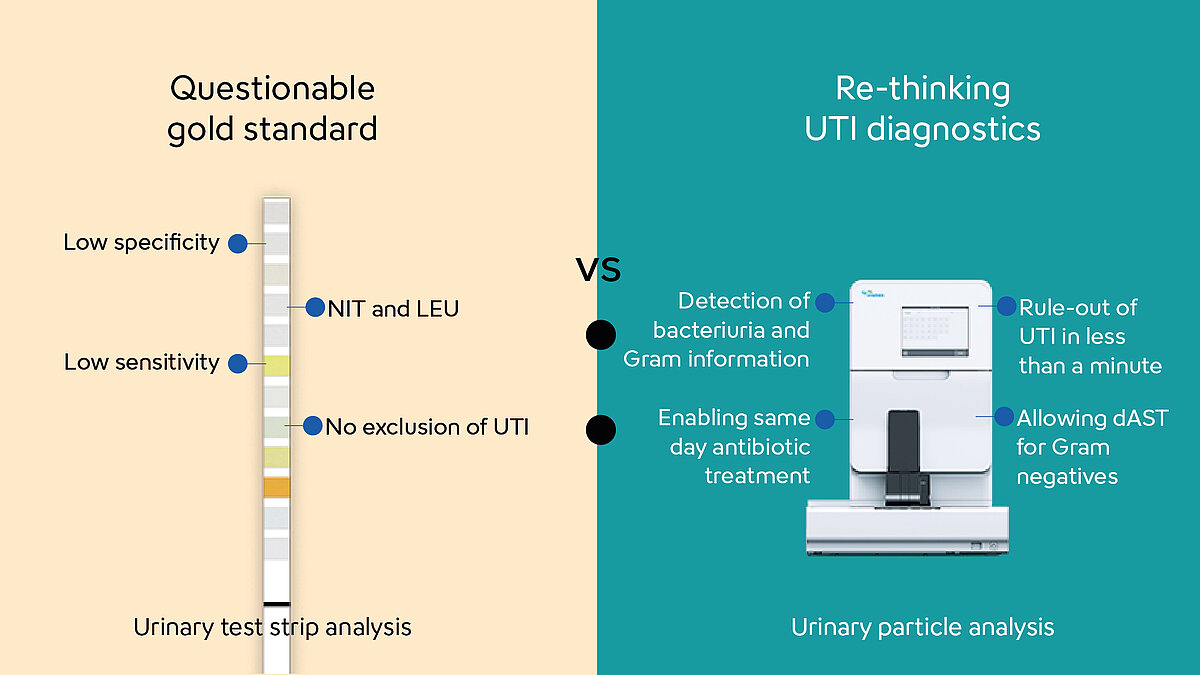
Zakażenie dróg moczowych (ZUM) w miejscu opieki nad pacjentem
Zakażenia dróg moczowych są przyczyną milionów konsultacji lekarskich i stanowią znaczne obciążenie dla systemów opieki zdrowotnej jak i społeczeństwa [1]. Właściwa diagnostyka ZUM jest czasochłonna, klinicyści często napotykają lukę informacyjną, w której informacje diagnostyczne nie są jeszcze dostępne, ale wymagane są już opcje leczenia. Często skutkuje to empirycznym przepisywaniem antybiotyków, mimo że aż 80% podejrzeń ZUM okazuje się negatywnych [2]. Tutaj innowacyjna technologia może pomóc zamknąć tę lukę informacyjną i poprawić wsparcie decyzji klinicznych w gabinecie lekarskim lub szpitalu.
Wyklucz ZUM w mniej niż minutę dzięki nowoczesnej diagnostyce
Zakażenie układu moczowego w warunkach szpitalnych
ZUM jest jednym z głównych zakażeń szpitalnych, a wcześniejsze badania wykazały, że ZUM może stanowić nawet do 40% wszystkich zakażeń szpitalnych (HAI) [3]. Zwłaszcza cewnikowanie jest głównym czynnikiem wywołującym ZUM (CAUTI), a zatem może skomplikować leczenie na OIT. Ze względu na fakt, że czas może mieć krytyczne znaczenie na podejmowanie decyzji dotyczących leczenia, posiadanie szybkiego i dokładnego sposobu na odróżnienie HAI od stanów zapalnych ma najwyższy priorytet.
Innowacyjne metody fluorescencyjnej cytometrii przepływowej umożliwiają wykluczenie HAI, takiego jak ZUM, lub uwiarygodnienie podejrzenia bakteriurii w mniej niż minutę.
Zakażenie układu moczowego w gabinecie lekarskim
Częste występowanie jak i samo podejrzenie ZUM w połączeniu z czasochłonnym charakterem właściwej diagnostyki tego schorzenia często skutkuje empirycznym przepisywaniem antybiotyków. Wymaga to późniejszego dostosowania terapii i sprzyja oporności na środki przeciwdrobnoustrojowe (AMR) [4].
Czas wykrycia próbek z ujemnym wynikiem pod względem ZUM można znacznie skrócić dzięki wykorzystaniu fluorescencyjnej cytometrii przepływowej do analizy moczu. Pozwala ona na wykluczenie ZUM w mniej niż minutę, co pomaga w ograniczeniu przepisywania antybiotyków w kontekście objawów podobnych do ZUM przy braku bakteriomoczu, tym samym zwalczając AMR [5].
W przypadku potwierdzonych przypadków bakteriurii fluorescencyjna cytometria przepływowa może dostarczyć dodatkowych informacji o klasyfikacji Grama wykrytych patogenów. Może to usprawnić proces diagnostyczny poprzez wspieranie bezpośredniego badania wrażliwości na antybiotyki (dAST), zwłaszcza w przypadku infekcji Gram-ujemnych. Poprawia to czasy odpowiedzi dla profili antybiotykowych i może umożliwić rozpoczęcie leczenia antybiotykowego już tego samego dnia [5].

Spojrzenie w przyszłość leczenia ZUM i stosowania antybiotyków
Pacjent poszukujący ulgi w złym samopoczuciu związanym z ZUM, w połączeniu z czasochłonną diagnostyką w celu podjęcia właściwych decyzji klinicznych, stwarzają dylemat w praktyce klinicznej, prowadząc do stosowania antybiotykoterapii u osób bez właściwej diagnostyki [4]. Niedawne badanie ujawniło, że pacjenci wolą wygodę i pewność metod diagnostycznych niż szybkość w kontekście AMR [6].
Aby kształtować postęp opieki zdrowotnej, dążymy do zbudowania mostu pomiędzy laboratorium a lekarzami za pomocą technologii diagnostycznej. Informacje diagnostyczne muszą być dostępne i zrozumiałe na wszystkich poziomach ścieżki podejmowania decyzji klinicznych. Umożliwi to szybkie i pewne wsparcie decyzji dotyczących leczenia ZUM. Poprawi to zarówno dylemat kliniczny, jak i doświadczenia pacjentów, a także rozwiąże rosnący wpływ oporności na środki przeciwdrobnoustrojowe poprzez ukierunkowane leczenie.
Jednym z przykładów jest badanie wrażliwości na antybiotyki (AST), które wykonuje się w celu określenia, który schemat przeciwdrobnoustrojowy jest szczególnie skuteczny w przypadku poszczególnych infekcji. Opracowywane są coraz nowsze technologie mające na celu usprawnienie i przyspieszenie procesu AST. Jednym ze sposobów, w jaki to się dzieje, jest pomiar tempa wzrostu komórek bakteryjnych w czasie rzeczywistym za pomocą chipów mikroprzepływowych i metod analizy obrazu. Próbkę umieszcza się na chipie mikroprzepływowym, a wszelkie obecne bakterie są wyłapywane w pułapki wielkości bakterii. Uwięzione bakterie są monitorowane, dzięki czemu czas ładowania daje oszacowanie gęstości bakterii w próbce. Wzrost bakterii jest monitorowany w każdej pułapce, z których niektóre zawierają predysponujący antybiotyk. Średnie tempo wzrostu oblicza się w czasie rzeczywistym, a bakterie uważa się za wrażliwe, jeśli ich wzrost jest należycie zahamowany.
Wgląd do laboratorium
Pracownicy laboratorium spędzają zazwyczaj do 40% swojego czasu na podejrzeniu ZUM, biorąc pod uwagę wszystkie zlecone posiewy. Pomimo swojej kosztownej i czasochłonnej natury, posiew moczu pozostaje złotym standardem w diagnostyce ZUM. Taki przepływ pracy może pochniać zasoby w laboratorium, a także powodować luki w komunikacji między laboratorium a lekarzami. Jak wspomniano wcześniej, 80% próbek podejrzanych o ZUM okazuje się negatywnych, dlatego szybka i niezawodna metoda wykluczenia ZUM może być motorem usprawniającym przepływu pracy w laboratorium i dodatkowo przekładać się na racjonalne zarządzanie środkami przeciwdrobnoustrojowymi.
Co po za analizą moczu
AMR – Dowiedz się więcej o oporności na środki przeciwdrobnoustrojowe i zaangażowaniu firmy Sysmex w jej zwalczanie na całym świecie. Zostań z nami #AMRfighterem!

Nadal chcesz wiedzieć więcej?
Sprawdź nasze inne treści naukowe, aby jeszcze bardziej zagłębić się w temat ZUM i innych powiązanych zagadnień.

Urinary tract infections (UTI) belong to the most common bacterial infections and, though suspected cases often turn out to be negative, contribute to high laboratory workloads and empiric prescription of antibiotics, a main driver antimicrobial resistance (AMR). This white paper reviews the strengths of the UF-series in ruling-out UTI, supporting its diagnosis and potential applications to further optimise the UTI laboratory workflow, aiming to fight AMR.

Diagnostics play a major role in the rational prescription of antibiotics. Well-known antimicrobial susceptibility tests (AST) are reliable tools for the phenotypic determination of resistance to antibiotics [6]. Several solutions to support AST performance are available on the market.
ŹRÓDŁA
[1] Foxman B (2014): Urinary tract infection syndromes: occurrence, recurrence, bacteriology, risk factors, and disease burden
[2] Keller, P. (2019): Ein neuer Schritt zur schnelleren Urinanalytik
[3] Kalsi, J., Arya, M., Wilson, P., & Mundy, A. (2003): Hospital-acquired urinary tract infection International journal of clinical practice, 57(5), 388–391.
[4] Pujades-Rodriguez et al. (2019): Lower Urinary Tract Infections: Management, Outcomes and Risk Factors for Antibiotic Re-prescription in Primary Care. EClinicalMedicine 14:23-31
[5] Gilboe, H. M., Reiakvam, O. M., Aasen, L., Tjade, T., Bjerner, J., Ranheim, T. E., & Gaustad, P. (2021): Rapid diagnosis and reduced workload for urinary tract infection using flowcytometry combined with direct antibiotic susceptibility testing. Plos one, 16(7), e0254064.
[6] Mott et al. (2020): A multinational European study of patient preferences for novel diagnostics to manage antimicrobial resistance. Applied Health Economics and Health Policy 18:69-79